
二类医疗器械进入注册变更高频期后,真正拖慢项目的往往不是单一技术难题,而是注册申报协同与量产切换之间的节奏失配。注册团队希望尽快递交,研发团队更关注验证通过,生产团队则被批次放行效率、交期和备料准确性牵引;三方都在完成各自目标,但项目却可能在补正、补测、转产和放行之间反复等待。
这类场景在医疗器械绩效管理中非常典型:资料已经提交,但验证证据未完全收口;样机验证通过,但转产一致性不足;生产已按窗口备料,却因标签说明书、工装或检验要求变化而返工。结果不是某一个部门“失误”,而是器械量产管理缺少围绕同一结果的共担口径。
因此,本文不讨论单部门KPI怎么优化,而是围绕“注册变更高频期如何让注册、研发、生产三团队共担申报进度、验证返工与上市切换窗口”展开,给出一套更适合医疗器械绩效落地的协同框架,帮助企业减少等待、返工和责任扯皮。
注册变更高频期,为何最容易拖慢二类器械量产节奏
判断很明确:变更多、文件多、窗口短时,单点最优通常会破坏整体最优。
二类器械在注册变更频繁阶段,设计、工艺、检验要求、标签说明书和生产文件往往需要同步调整。表面看每项工作都能找到负责人,但一旦缺少统一的注册变更里程碑,项目就会出现“递交完成但后端未就绪”的断层。
这也是很多企业在医疗器械绩效管理中反复遇到的问题:注册以递交时点为主,研发以验证通过为主,生产以排产达成和放行为主。每个指标都合理,但彼此之间没有被同一个上市切换窗口约束,最终导致补正响应、验证返工管理和首批放行互相掣肘。
三团队协同失效的根因:申报导向、技术导向与交付导向相互割裂
核心问题不是“谁做得不够”,而是“谁也不对整体切换结果负责”。
在很多项目中,注册团队关注资料一次提交完整率和补正响应周期,研发团队关注样机转产一致性和验证一次通过率,生产团队关注备料、试产、批次放行效率和交期达成。若这些目标没有被统一到同一时间轴上,就会出现三类典型割裂:
- 注册节点提前,但验证证据和一致性说明滞后,导致申报已递交、内容仍需回补。
- 研发验证完成,但未把变更后的工艺、检验、标签说明书与生产版本充分挂钩,导致首批转产放大偏差。
- 生产为保障上市窗口提前备料排产,但前端设计或文件仍处于变化中,形成备料返工和试产重启。
这正是注册申报协同失效的典型表现:不是流程没有,而是里程碑、责任口径和触发规则没有打通。
典型痛点与案例:从“已递交”到“未切换成功”的失控路径
以下两组场景,基本覆盖了二类器械变更高频期最常见的业务失控方式。
案例一:资料已递交,但验证未收口,生产已提前备料
问题:某企业在注册变更提交前,以递交时点为核心目标推进资料封版。注册团队完成了资料组织,研发侧部分补测结论尚未完全固化,生产端则按原计划启动备料与工装准备。
直接影响:后续补正意见要求补充一致性说明后,验证记录、工艺文件与生产准备物料需要同步回退。表面是补正工作增加,实质上是验证返工管理失控。
连锁反应或管理后果:资料重整、试产延后、备料返工同时发生,项目团队开始围绕“是否该先递交”“谁批准提前备料”“补测责任归谁”反复拉扯。最终,申报进度没有真正领先,反而拖累上市切换窗口。
案例二:标签说明书、检验要求与关键工序参数同时调整,首批放行被拉长
问题:某产品在变更过程中,标签说明书、检验要求和关键工序参数同时发生变化。研发已完成技术确认,但生产未将首批放行条件与新版本文件完全挂钩。
直接影响:试产批次偏差记录增加,关键工序执行与新要求存在不一致,批次放行效率明显下降。
连锁反应或管理后果:问题归因在研发与生产之间反复摇摆,工序偏差控制从现场执行问题演变成版本管理问题,后续还可能引出体系稽核整改压力,影响后续批次复制和不良事件闭环质量。
案例三:各部门都完成KPI,但首批量产切换仍然失败
问题:注册按时递交,研发按计划完成验证,生产也完成了试产安排,看上去每个部门都“交卷”了。
直接影响:由于关键节点之间缺少统一验收口径,试产偏差关闭周期被拉长,重复验证工时损失上升,批次放行仍然无法稳定。
连锁反应或管理后果:企业在复盘时只能看到部门成绩,看不到项目损失,导致下一轮变更仍按旧方式推进,器械量产管理持续依赖个人协调。
共担绩效设计的核心判断:先统一里程碑,再统一责任口径
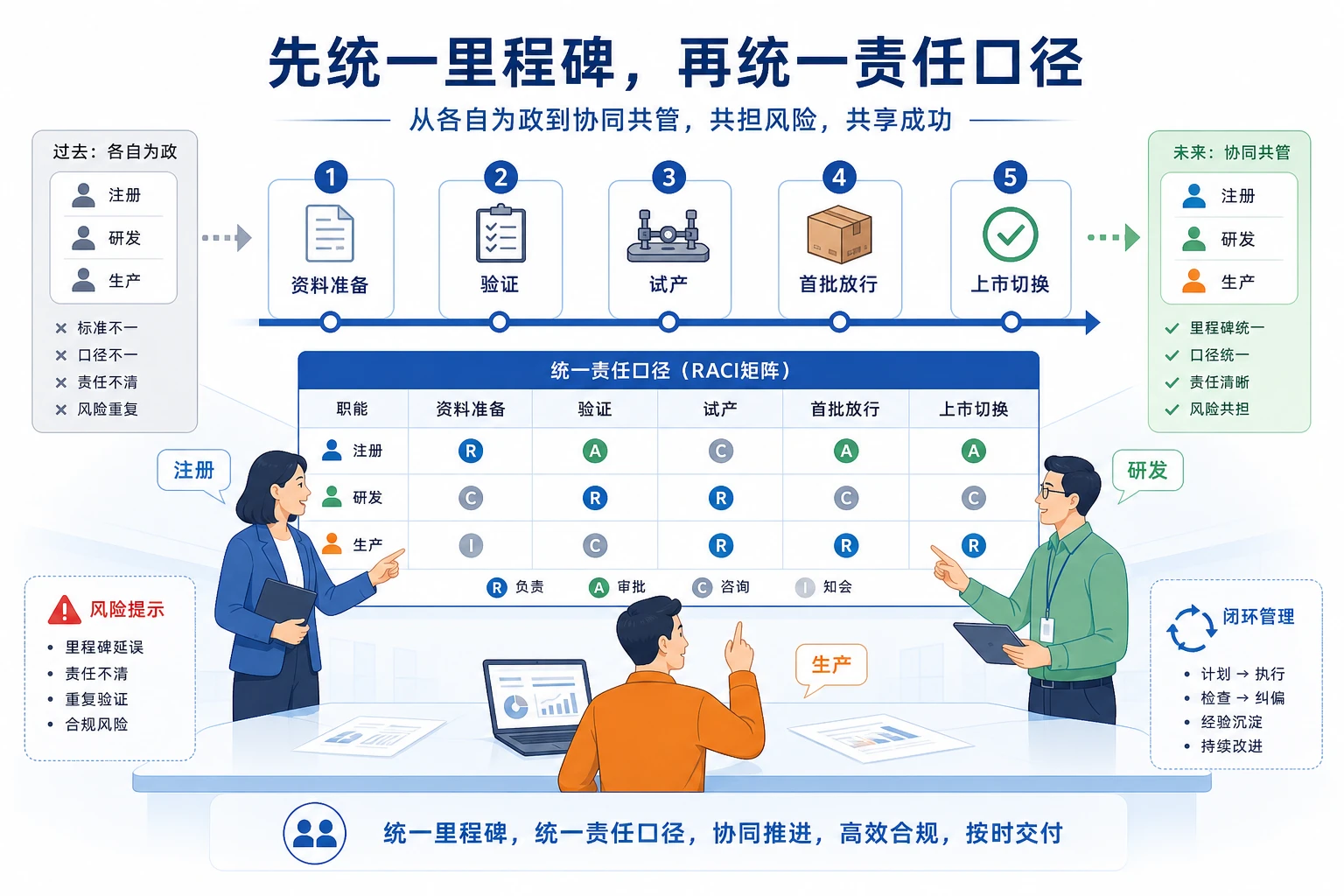
要解决问题,首先要接受一个现实:在变更高频期,不能再用单部门最优逻辑管理量产切换。
更有效的医疗器械绩效设计,应以注册变更项目或产品族为基本单元,把资料准备、验证、试产、首批放行和上市切换纳入同一时间轴;同时设置共担指标与部门指标并行的结构,让“递交完成”不再等于“项目完成”。
| 绩效模块 | 共担目标 | 重点指标 | 主要责任团队 | 触发扣分/预警情形 |
|---|---|---|---|---|
| 申报进度 | 保证递交与补正节奏可控 | 资料一次提交完整率、补正响应周期、关键节点准时率 | 注册、研发 | 递交后关键证据回补、补正超期、版本不一致 |
| 验证闭环 | 避免补测和重复验证扩散 | 样机转产一致性、验证一次通过率、重复验证工时损失 | 研发、生产 | 验证结论未固化即转产、重复验证、试产条件变化未同步 |
| 试产与转产 | 保障首批切换稳定 | 试产偏差关闭周期、首批达成率、关键工序偏差控制 | 生产、研发 | 关键偏差未闭环、工装/工艺文件未同步、备料返工 |
| 放行与上市切换 | 兼顾速度与合规 | 批次放行周期、首批放行通过情况、上市切换窗口达成 | 生产、质量、注册 | 放行条件不完整、标签说明书版本错配、上市延后 |
| 后评估与闭环 | 把问题沉淀为模板 | 不良事件闭环时效、体系稽核整改完成率、项目复盘完成率 | 质量、注册、生产、研发 | 同类问题重复发生、整改无证据、责任口径不清 |
申报进度模块:避免“只追递交,不追闭环”
注册申报协同最常见的偏差,是把递交视为阶段终点,而不是阶段闸门。资料一次提交完整率、关键节点准时率当然重要,但必须叠加“递交后是否引发后端回退”的约束。
因此,申报进度指标不能只看时间,还应看内容成熟度。比如,凡是递交后因验证证据未收口、版本不一致、标签说明书未同步而触发回补,就不应仅由注册团队承担后果,而要回溯到相关共担团队。
验证返工管理:把责任量化到研发与生产协同过程
验证返工管理的关键,不是简单统计“返工次数”,而是识别返工是由技术结论不稳定、转产一致性不足,还是试产条件变化未同步造成。
更可执行的做法,是把样机转产一致性、验证一次通过率、重复验证工时损失放在同一模块中看。这样可以避免研发只对“验证完成”负责,而生产只对“试产执行”负责,最终没人对重复验证的成本负责。
上市切换窗口:用首批放行结果检验前端协同质量
上市切换窗口不是生产部门单独守住的,而是前端决策质量在后端的集中体现。若标签说明书、检验要求、工艺文件和放行条件未完全对齐,批次放行效率必然被拖慢。
所以,首批达成率、批次放行周期和关键工序偏差控制,应被视为跨部门结果指标,而不是单纯的制造执行指标。这也是器械量产管理从“看节点”走向“看结果”的关键一步。
不良事件闭环与体系稽核整改:把切换后的问题纳入绩效回路
很多企业只考核变更前和首批切换阶段,却忽略切换后的问题闭环。实际上,变更后的早期不良反馈、偏差复发、文件执行不一致,往往最能反映前期协同质量。
将不良事件闭环、体系稽核整改和项目复盘纳入医疗器械绩效体系,可以避免问题只停留在现场层面,而无法沉淀为下一轮变更的标准动作。
传统方式 vs 共担机制:差异不在表面流程,而在责任设计
判断很简单:流程图相似,并不代表协同能力相同,差别往往出在指标口径和触发规则上。
| 对比维度 | 传统分部门考核 | 共担绩效机制 |
|---|---|---|
| 项目主线 | 按部门任务推进 | 按注册变更里程碑和量产切换窗口推进 |
| 责任归属 | 各自对本部门KPI负责 | 对共同节点与共同结果共同负责 |
| 进度判断 | 重递交、重完成打卡 | 重闭环、重后端是否可执行 |
| 返工管理 | 返工后再协调归因 | 提前设置重复验证、版本错配、关键偏差等触发规则 |
| 放行管理 | 放行周期主要由生产承担压力 | 批次放行效率作为跨部门协同结果评价 |
| 经验沉淀 | 复盘依赖个人经验 | 按项目沉淀模板、责任口径和权重策略 |
从实践看,这类机制未必让每个单点任务都明显缩短,但通常可见的收益是等待减少、返工减少、节点透明度提升,以及首批切换的可控性增强。对于上市窗口紧、变更多的项目,这种收益往往比单个部门的局部提速更重要。
实施建议:按不同对象与阶段配置医疗器械绩效框架
最有效的做法不是一次性铺开全部规则,而是按组织成熟度和业务场景分层落地。
场景一:变更频繁、项目并行多的企业
适用对象:产品线较多、注册变更项目并行推进、窗口管理压力大的企业。
优先模块:先上线统一里程碑、关键节点准时率、资料一次提交完整率、首批放行节点看板。
落地难点:项目归口不清,部门之间对同一节点的定义不一致,容易出现统计口径争议。
预期收益:先解决信息断层问题,让管理层看到“递交完成但后端未就绪”的真实风险位置。
场景二:验证返工高发、试产重复启动的企业
适用对象:补测频繁、样机转产一致性不足、验证返工管理压力大的企业。
优先模块:优先建立验证一次通过率、重复验证工时损失、试产偏差关闭周期、备料返工触发规则。
落地难点:返工责任容易被模糊处理,研发与生产都能解释“不是本部门单独造成”。
预期收益:把返工从结果描述转为过程责任识别,减少反复试错和跨部门拉扯。
场景三:首批放行慢、上市切换窗口经常错失的企业
适用对象:生产切换频繁、首批批次放行效率波动大、市场窗口压缩明显的企业。
优先模块:首批达成率、批次放行周期、工序偏差控制、标签说明书与放行条件同步校验。
落地难点:生产端容易被动背压,但真正原因可能在前端变更评审和版本切换。
预期收益:把上市切换窗口从“制造交付问题”升级为跨部门经营指标,更利于管理层统一资源配置。
场景四:体系化管理起步较晚、希望逐步规范的企业
适用对象:目前仍依赖会议推进和人工跟催,尚未形成统一项目台账的企业。
优先模块:先从项目制台账、责任人、证据留痕和问题闭环做起,再逐步叠加权重和自动触发考核。
落地难点:一开始容易把系统建设理解为“多填表”,导致业务团队抵触。
预期收益:先把协同过程看见、记录下来,再逐步沉淀为可复用的器械量产管理模板。
落地顺序建议:先抓共同节点,再抓权重设计,最后做复盘沉淀
对于二类器械注册变更高频期而言,真正有效的医疗器械绩效设计,不是把注册、研发、生产三方都考得更细,而是让三方开始为同一个切换结果负责。先统一注册变更里程碑,再统一验证闭环和首批放行口径,最后通过触发规则把补正、返工、偏差和闭环责任连接起来,注册申报协同才会从“靠人盯”走向“靠机制跑”。
从长期看,企业要提升的不只是批次放行效率或某一次上市切换窗口达成率,而是建立一套能够在高频变更下持续复用的器械量产管理方法。只有把申报时效、验证质量、工序偏差控制、体系稽核整改和不良事件闭环放进同一框架,跨部门协同才能真正成为经营能力,而不是项目运气。
总结与建议
二类器械进入注册变更高频期后,企业真正需要优化的不是某一个部门的速度,而是围绕申报、验证、试产、放行和上市切换建立同一套结果导向的协同机制。对医疗器械绩效而言,只有把注册申报协同、验证返工管理、批次放行效率和工序偏差控制放到同一时间轴上,才能避免“资料已递交、现场未就绪”或“各部门都达标、项目仍失控”的典型问题。
更可执行的做法,是先从共同里程碑和共同触发规则入手,再逐步细化权重分配与扣分逻辑。建议企业优先建立三类基础动作:一是统一版本、节点和证据口径,减少补正回补与转产返工;二是把首批放行结果和上市切换窗口纳入跨部门共担指标,而非仅压在生产端;三是将不良事件闭环、体系稽核整改和项目复盘纳入后评估,形成可复用的器械量产管理模板。这样,绩效体系才不只是考核工具,而会真正变成支撑高频变更落地的经营机制。
常见问题
医疗器械绩效体系里,为什么不能只按注册、研发、生产分别考核
1. 分部门考核容易让团队只对本环节交付负责,却不对最终上市切换结果负责,这会放大等待和返工。
2. 在注册变更频繁阶段,资料递交、验证收口和量产放行彼此强依赖,单点达标并不代表项目真正可落地。
3. 更有效的方式是设置共担指标与部门指标并行,让申报时效、验证质量和首批量产结果被同一口径约束。
注册申报协同做得好,通常应优先观察哪些预警信号
1. 如果资料递交后仍频繁出现关键证据回补,说明前端成熟度判断不足,协同质量并不稳定。
2. 如果补正响应主要依赖临时拉会和人工催办,而不是基于统一版本和节点清单推进,后续项目仍会重复失控。
3. 如果生产已提前备料或排产,但标签说明书、检验要求和工艺文件还在变动,通常意味着申报与量产窗口没有真正对齐。
器械量产管理中,批次放行效率下降一定是生产执行问题吗
1. 不一定,批次放行效率下降往往是前端设计变更、文件切换、检验条件更新和现场执行共同作用的结果。
2. 如果放行资料不完整、版本错配或关键工序参数未同步,即使生产现场执行稳定,放行周期也会被拉长。
3. 企业应把批次放行效率定义为跨部门结果指标,这样才能准确识别问题源头,而不是让生产单独背压。
验证返工管理应该如何区分研发责任和生产责任
1. 判断重点不应只看返工是否发生,而应看返工是由技术结论不稳定、样机转产一致性不足,还是试产条件变更未同步造成。
2. 研发侧更适合承担验证方案完整性、技术结论稳定性和设计输出可转产性的责任口径。
3. 生产侧更适合承担试产执行一致性、工装工艺落地和偏差闭环时效等责任口径。
4. 对于重复验证工时损失这类结果,建议设为共担指标,避免责任被长期模糊化。
体系稽核整改和不良事件闭环,为什么要放进注册量产协同绩效里
1. 因为很多协同问题不会在递交当下暴露,而会在首批上市后通过偏差复发、不良反馈或稽核发现集中体现。
2. 把体系稽核整改和不良事件闭环纳入绩效,可以检验前期变更是否真正转化为稳定量产能力。
3. 这类后评估指标还能帮助企业把一次性问题沉淀为标准模板,降低下一轮注册变更和量产切换的试错成本。
本文由 i人事 医疗器械生产人力数字化解决方案团队 联合出品。如需预约演示或获取行业案例,请访问i人事官网。
原创文章,作者:hr,如若转载,请注明出处:https://docs.ihr360.com/blog/925367
