
医疗器械量产初期,最容易出现的不是“没人努力”,而是努力方向被错误绩效牵引。车间主管一边要盯批次放行效率,避免首批量产阶段因补记录、返工返检、QA排队拖慢交付兑现;另一边又必须守住关键工序记录、偏差上报、纠正预防和变更执行的底线,这使医疗器械绩效设计天然比一般制造更复杂。
尤其在注册转量产阶段,注册申报协同、验证安排、物料切换、体系稽核整改、QA放行等待等因素会同时影响结果。如果奖金只看产量或交期,容易逼出带病流转;如果只看零偏差,又可能把问题压到现场不进入系统;如果只看最终交付兑现,跨部门责任会被混成一团,车间主管奖金失去公允性和约束力。
因此,这篇文章不讨论单一KPI,而是聚焦一套更适合器械量产管理的联动方法:如何把质量底线、批次放行效率、工序偏差控制、跨部门注册申报协同和交付兑现放进同一套可追溯、可归因、可执行的奖金模型中。
量产初期为什么最容易出现医疗器械绩效失真
判断很明确:注册转量产阶段的波动不是异常,而是常态,所以沿用稳定期的单一考核方式,往往会直接放大管理偏差。
这一阶段的批次放行效率,并不只由生产快慢决定。放行起止口径是否统一、首批和验证批是否单独统计、异常批次是否剔除、QA节点是否独立核算,都会决定数据是否可用。如果这些前提不清,车间主管为了保奖金,最容易去挤压记录、检验、偏差处理等看起来“慢”的动作。
与此同时,工序偏差控制也不能用“偏差越少越好”简单替代。对医疗器械生产而言,真正应被鼓励的是及时上报、及时调查、及时关闭,而不是表面上的零异常。否则,偏差不透明会比偏差数量高更危险。
车间主管奖金设计的三个核心判断原则
先定原则,再定指标,否则任何评分表都会走向失真。
1. 质量底线先于效率结果
凡涉及重大偏差、关键记录缺失、未经批准继续流转、关键工序失控等情形,应先触发质量一票否决。也就是说,批次放行效率再高、交付兑现再好,都不能覆盖底线违规。
2. 注册申报协同约束必须前置
量产初期常见的注册资料补充、工艺验证插单、物料替代审批、标签说明书版本切换,都会影响生产与放行节奏。若不把注册申报协同纳入绩效口径,交付延误会被简单算到生产头上,造成奖金失真。
3. 交付结果不能脱离过程控制
交付兑现是结果,但结果必须建立在可审计的过程数据上。否则,表面完成订单,背后却可能积累返工返检、CAPA滞后、不良事件闭环延迟和体系稽核整改积压,长期成本更高。
常见失衡案例:只看产出、只抓质量或只保交期都会出什么问题
典型问题往往不是指标本身错,而是指标只覆盖了局部管理目标。
案例一:只考核批次放行效率,结果并没有真正提速
某企业在新品注册完成后进入首轮量产,车间主管奖金主要绑定产出和交期。为了提升批次放行效率,前段装配和中间检验节点被压缩,批次更快流到QA,但偏差记录滞后、返工返检增加,月末集中暴露问题。
直接影响:表面上生产流转更快,实际有效放行周期并未缩短。
连锁反应:QA端等待补记录、补调查,返工返检比例上升,生产与QA互相归责,最终交付兑现和医疗器械绩效都变差。
案例二:把“零偏差”当核心奖金指标,反而逼出瞒报和延报
某团队为压住异常数量,把车间主管奖金与“零偏差”强绑定。报表短期看似改善,但一线更倾向把轻微异常留在现场处理,不愿正式发起偏差流程。
直接影响:工序偏差控制表面更好,实际上重复性问题缺少正式记录。
连锁反应:后续批次稳定性下降,调查发现真正的问题不是偏差过多,而是偏差不透明、CAPA关闭不及时,不良事件闭环基础也被削弱。
案例三:只保交付兑现,排程越来越乱
某量产爬坡项目将交付兑现作为主管奖金核心,却未区分注册变更、工艺验证插单、物料切换审批和QA放行等待等因素。为保奖金,车间不断要求提前开工、并行流转。
直接影响:排程频繁变动,现场忙而无序。
连锁反应:返工与等待并存,生产、QA、计划、注册之间责任边界模糊,最后既伤交期也伤质量。
奖金联动总模型:底线指标、结果指标与协同指标怎么组合
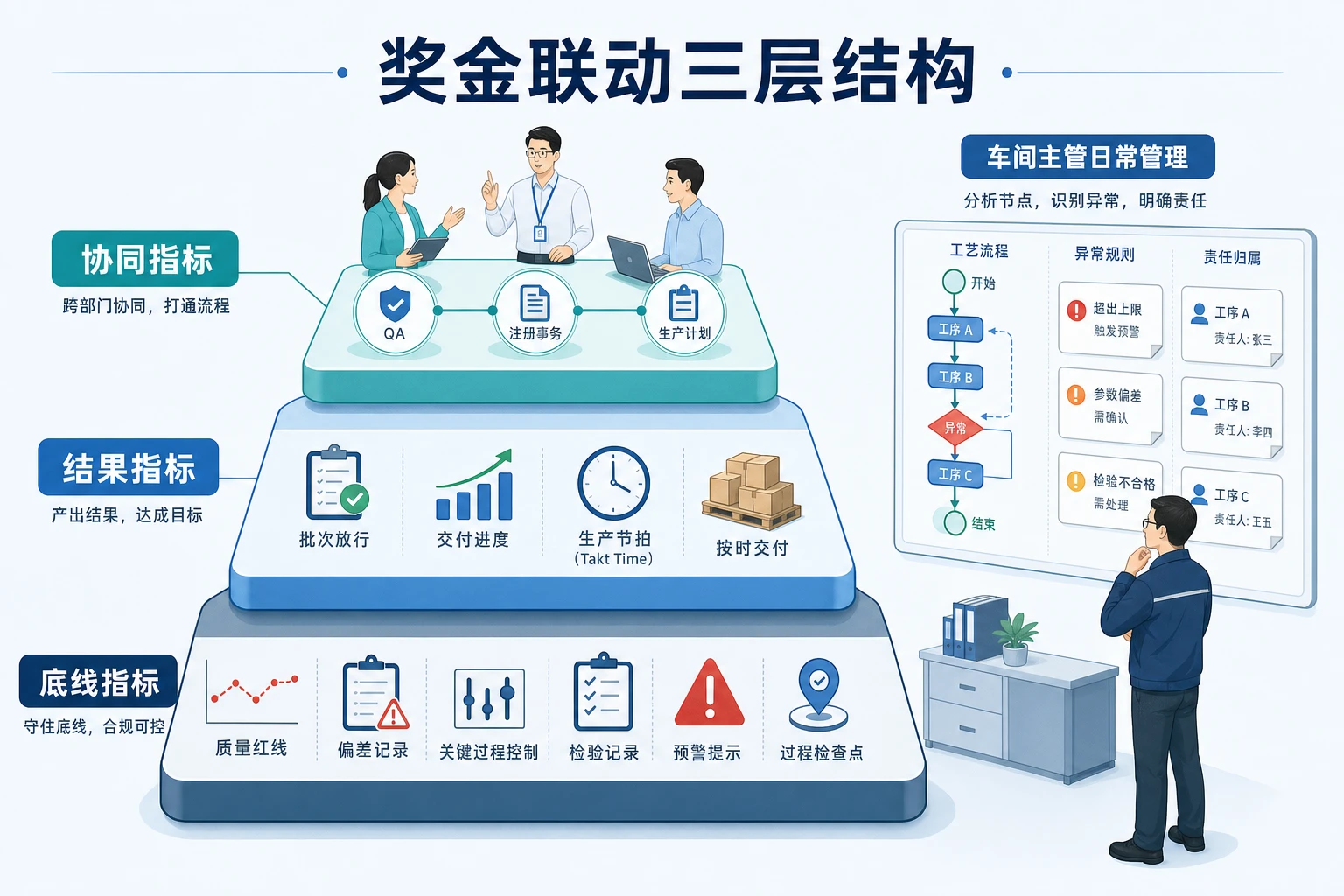
更稳妥的设计思路,是把车间主管奖金拆成三层:先守红线,再看结果,最后校正协同责任。
| 指标层级 | 核心内容 | 建议权重区间 | 数据口径重点 | 红线/扣罚逻辑 | 适用场景 |
|---|---|---|---|---|---|
| 底线指标 | 重大偏差、关键记录缺失、未经批准流转、关键工序违规 | 一票否决或单独门槛 | 按批次、工序、事件等级追溯 | 触发即取消当期相关奖金或大幅扣减 | 首批量产、验证批、风险爬坡期 |
| 结果指标 | 批次放行效率、交付兑现、返工返检率、计划达成 | 40%—60% | 需明确放行起止口径、异常批次剔除规则 | 超阈值分档扣减,避免唯速度论 | 量产导入后至稳定放量阶段 |
| 协同指标 | 偏差及时上报率、CAPA关闭率、变更执行配合、体系稽核整改完成率 | 20%—40% | 按部门责任分摊,保留过程证据 | 逾期未闭环或配合失效按责任扣分 | 跨部门协同复杂的注册转量产阶段 |
在医疗器械绩效实践中,这类三层结构比单一KPI更能解释真实经营状态。表格附近最关键的动作,不是把权重写满,而是把统计节点、例外规则、责任归因先定清楚。
批次放行效率指标如何定义,才不会逼出带病流转
建议把“有效放行周期”而不是“纯生产完成时间”作为核心口径。起点可设为批次达到规定完工与记录齐套条件的时间,终点设为QA完成放行判定的时间。这样可以避免把尚未准备好的批次提前推给QA,制造虚假提速。
同时应设置异常批次剔除规则,例如验证批、注册变更涉及批、物料替代审批批、重大偏差调查批,可按单独池统计。否则不同批次类型混算,会误导车间主管奖金。
关键工序偏差控制指标如何设计,才能真正约束过程波动
工序偏差控制不宜只看“数量”,而应至少包括偏差及时上报率、重复性偏差发生情况、分级偏差关闭及时率、CAPA有效关闭率。对重复性偏差应加重扣分,因为它代表过程波动没有被真正消除。
对一线最重要的信号是:如实上报不直接等于扣罚,瞒报、延报、关闭不及时才是重点约束对象。这样才能让偏差数据成为管理抓手,而不是现场压力来源。
交付兑现指标如何与注册申报协同和生产排程联动
交付兑现应区分可控与不可控影响。生产组织不当、排程执行偏差、返工返检引发延误,可计入车间责任;而注册申报协同、标签版本切换、验证安排、外部审批等待等因素,应进入协同归因机制,而不是全部压到车间主管奖金上。
这类处理有助于减少跨部门甩锅,也能让计划、QA、注册、工艺和供应链围绕同一交付口径协作。
体系稽核整改与不良事件闭环为什么也要纳入奖金联动
对医疗器械生产来说,奖金不能只奖励“出货”,还要奖励“把问题关住”。若体系稽核整改长期逾期,或不良事件闭环反馈迟缓,说明过程管理仍有漏洞。把整改完成率、关闭及时性纳入协同指标,能把短期结果和长期合规能力连接起来。
版本化口径管理是量产初期最容易被忽视的模块
同一个产品在首批、验证批、工艺切换批、稳定量产批下,考核标准不应完全一致。成熟做法通常会按阶段切换权重和阈值,例如量产初期更重质量底线与协同闭环,稳定期再逐步提高批次放行效率和交付兑现的权重。
方法表格:车间主管绩效指标库、权重区间与红线示例
下面这组指标更适合作为实施时的基础库,便于在全面绩效系统中做版本化配置。
| 指标名称 | 定义说明 | 建议权重 | 主要数据来源 | 红线规则 | 适用对象/场景 |
|---|---|---|---|---|---|
| 质量一票否决 | 重大偏差、关键记录缺失、未经批准流转等 | 门槛项 | 偏差系统、批记录、QA审核 | 触发即否决或重扣 | 所有车间主管 |
| 有效批次放行周期 | 从记录齐套完工到QA完成放行的有效时长 | 15%—25% | MES/批记录/QA放行记录 | 异常批次按规则剔除或单列 | 量产导入、稳定放量 |
| 关键工序偏差及时上报率 | 规定时限内完成偏差发起的比例 | 10%—15% | 偏差系统、工序记录 | 瞒报、延报单独扣罚 | 关键工序负责人、车间主管 |
| 重复性偏差控制 | 同类偏差重复发生情况及改善成效 | 5%—10% | 偏差台账、CAPA台账 | 重复发生超阈值加重扣分 | 爬坡期产品线 |
| 返工返检率 | 因记录、工艺、检验问题导致返工返检的比例 | 10%—15% | 返工单、检验记录 | 重大返工关联质量门槛 | 首批量产与爬坡阶段 |
| 交付兑现率 | 剔除经确认的非生产责任后订单按期达成情况 | 15%—25% | 计划排程、订单、放行记录 | 需有责任分摊规则 | 交付压力较高产线 |
| CAPA关闭率 | 纠正预防措施按期关闭比例 | 5%—10% | CAPA系统 | 逾期关闭持续扣分 | 跨部门协同场景 |
| 体系稽核整改完成率 | 与车间相关整改项的按期完成情况 | 5%—10% | 稽核整改台账 | 逾期未完成扣分 | 体系提升期 |
传统方式 vs 联动机制:量化收益怎么判断
如果不强行给出脱离场景的精确数字,更稳妥的判断是:相比传统单一指标考核,联动机制通常可见三类改进。
| 比较维度 | 传统单一考核 | 联动式医疗器械绩效方案 |
|---|---|---|
| 批次放行效率 | 容易通过前移流转、压缩记录获得表面改善 | 更关注有效放行周期,减少“快流转、慢放行” |
| 工序偏差控制 | 偏差数量可能下降,但瞒报和延报风险上升 | 强化及时上报、分级处理、重复性偏差治理 |
| 交付兑现 | 常把所有延期压给生产,责任失真 | 通过责任分摊和协同指标提高兑现的可解释性 |
| 跨部门关系 | 生产、QA、注册、计划互相归责 | 以统一口径和证据链减少扯皮 |
| 长期改进 | 奖金只用于分钱,难以反哺管理 | 绩效可联动CAPA、整改、例会复盘形成闭环 |
从实际管理效果看,这种机制通常更有利于稳定批次放行效率、改善工序偏差控制透明度,并提升交付兑现的可追责性。对车间主管而言,奖金逻辑更清晰;对管理层而言,数据也更接近真实经营状态。
实施建议:按组织阶段与适用对象分步落地
落地顺序比模型本身更重要,尤其在量产初期,不建议一步到位把所有指标同时压实。
场景一:新品首批量产/验证批阶段
适用对象:新品车间主管、工艺负责人、QA现场负责人。
优先模块:质量一票否决、偏差及时上报、异常批次剔除规则、注册申报协同节点。
落地难点:放行起止口径不统一,首批和常规批混算,验证活动频繁插单。
预期收益:先把数据边界划清,避免用错误指标打击一线,也避免为追求批次放行效率牺牲合规。
场景二:量产爬坡阶段
适用对象:车间主管、计划负责人、QA放行团队、供应链协同岗位。
优先模块:有效批次放行周期、返工返检率、重复性偏差控制、交付兑现责任分摊。
落地难点:产线波动大,物料切换和排程调整频繁,责任边界容易模糊。
预期收益:把“速度、稳定、交付”放入同一框架,减少月末集中暴露问题。
场景三:进入相对稳定放量阶段
适用对象:成熟产线车间主管及制造管理层。
优先模块:提高交付兑现和放行效率权重,同时保留体系稽核整改、不良事件闭环、CAPA关闭率等协同项。
落地难点:容易因为产能稳定而忽视过程纪律,导致旧问题反复出现。
预期收益:让医疗器械绩效从短期奖金工具,逐步升级为持续改进机制。
场景四:系统化建设阶段
适用对象:人力、制造、质量、注册、IT联合项目组。
优先模块:指标版本管理、批次/工序/订单维度追溯、红线规则、协同评价、整改联动。
落地难点:历史口径不统一,部门间对“谁负责”理解不同。
预期收益:把车间主管奖金从经验判断变成可配置、可追责、可复盘的数据机制。
把车间主管奖金做成长期有效的管理机制
对医疗器械生产企业而言,量产初期最怕的不是指标多,而是指标错。真正合理的车间主管奖金,不应只奖励批次放行效率,也不能只盯工序偏差控制,更不能脱离注册申报协同和交付兑现去看结果。
更可行的顺序是:先设质量底线,再定义有效结果,最后补上协同归因;先统一口径,再谈权重;先让问题透明,再追求速度优化。只有这样,医疗器械绩效才不会把一线推向瞒报和带病流转,而是推动批次放行效率、工序偏差控制与交付兑现进入同一套可持续改进的管理闭环。
总结与建议
医疗器械量产初期的绩效设计,核心不在于把更多指标塞进奖金公式,而在于先解决口径、边界和责任归因。对车间主管奖金而言,真正可执行的做法是先设质量一票否决,再用批次放行效率、交付兑现等结果项衡量产出,最后用工序偏差控制、CAPA关闭、体系稽核整改等协同项修正过程表现。这样才能避免“放行提速了,问题却被后移了”的假改善。
实际落地时,建议企业优先完成三件事:第一,统一有效放行周期的起止定义,并将验证批、注册变更批、重大偏差调查批单列统计;第二,把工序偏差控制从“压数量”改为“抓及时上报、重复性治理和按期关闭”;第三,建立跨部门责任分摊机制,避免将注册申报协同、QA等待和外部审批全部压到生产端。只有数据口径稳定、红线规则明确、协同证据留痕,医疗器械绩效体系才会真正支撑量产管理,而不是制造新的内部冲突。
常见问题
医疗器械绩效体系里,为什么不能把批次放行效率单独作为车间主管奖金核心指标
1. 批次放行效率如果脱离质量门槛,容易驱动现场提前流转、压缩记录和延后偏差处理,最终形成表面提速、实际变慢。
2. 医疗器械生产的放行结果不仅受生产节拍影响,还受QA审核、记录齐套、异常调查和注册变更执行影响,单一考核会导致责任失真。
3. 更合理的做法是把放行效率放在结果项中管理,同时用质量红线和协同项对冲短期速度冲动。
工序偏差控制指标怎么设,才能避免一线为了奖金少报或晚报
1. 不要把偏差数量简单等同于管理好坏,而应重点考核及时上报率、分级处理及时率、重复性偏差发生率和CAPA关闭效果。
2. 对如实上报的轻微偏差应弱化直接扣罚,对瞒报、延报和重复发生但未改善的情况加重处理,才能形成正确导向。
3. 现场管理者需要看到明确信号:透明暴露问题是管理贡献,刻意隐藏问题才是绩效风险。
量产初期如何判断批次放行效率下降,到底是生产问题还是注册申报协同问题
1. 应先拆分放行周期节点,区分生产完工、记录齐套、QA接收、QA审核、偏差调查和最终放行几个时间段。
2. 如果延迟主要集中在版本切换、验证插单、物料替代审批或注册资料补充环节,就不应全部计入车间主管责任。
3. 只有把订单、批次、变更和审批记录关联到同一证据链中,交付延误的归因才具备可审计性。
医疗器械绩效落地时,首批量产和稳定量产的奖金权重需要一样吗
1. 通常不建议完全一样,因为首批量产阶段的不确定性更高,质量底线、偏差透明度和注册协同的重要性明显高于单纯效率。
2. 在量产爬坡期,可以适当提高工序偏差控制、返工返检率和协同整改的权重,等过程稳定后再提升交付兑现和放行效率占比。
3. 采用阶段化或版本化权重设置,更符合医疗器械量产管理的真实节奏,也更容易被一线接受。
体系稽核整改和不良事件闭环为什么也适合纳入车间主管绩效
1. 这两类指标能反映车间是否真正把问题关住,而不仅是把产品赶出去,对医疗器械生产的长期合规能力非常关键。
2. 如果稽核整改长期逾期,或不良事件相关改进没有回到工序控制中,说明现场管理还存在系统性漏洞。
3. 将其作为协同指标纳入奖金联动,可以把短期交付结果与长期质量改进连接起来,避免绩效只奖励眼前产出。
本文由 i人事 医疗器械生产人力数字化解决方案团队 联合出品。如需预约演示或获取行业案例,请访问i人事官网。
原创文章,作者:hr,如若转载,请注明出处:https://docs.ihr360.com/blog/925325
